初始循环中锂的损失会显著降低锂离子电池的能量密度。一般常用阳极预锂化解决该问题,但该方法存在高化学反应性、环境稳定性差和工艺复杂等问题。本文报告了一种简便的阴极预锂化方法,该方法具有高预锂化效率,并且与现有锂离子电池技术具有良好的兼容性:一种由过渡金属和氧化锂的纳米级混合物组成的阴极预锂化添加剂,理论预锂化容量高达 800mAh/g、2.7Ah/cm3。在全电池中,具有 4.8% Co/Li2O 添加剂的 LiFePO4 电极的总容量比原始 LiFePO4 电极的总容量高 11%。正极添加剂的使用提供了一种有效的途径来补偿高容量负极材料的大量初始锂损失,提高现有锂离子电池的电化学性能。
可充电锂(Li)离子电池目前在便携式电子市场占据主导地位,在电动汽车、电网规模储能和可再生能源存储方面具有巨大潜力。商用锂离子电池由两个电极组成:嵌入的锂过渡金属氧化物阴极(例如 LiCoO2、LiMn2O4 和 LiFePO4)和石墨阳极。在第一次充电过程中,由于在阳极表面形成SEI,通常会消耗正极5-20%的活性锂,从而导致较低的首效和较高的初始不可逆容量损失。电化学预锂化是一种有效的补锂方法,例如直接将 Sn_C 电极与被电解质溶液润湿的锂箔直接接触,并对硅纳米线电极/锂箔半电池放电;但如此复杂的操作过程和它们在环境大气中的不稳定性并不适合工业化放大。另一种补锂方法是增加额外的正极材料。然而,由于现有正极材料的比容量低(<200mAh/g),需要增加大量的额外正极材料,这显然降低了整个电池的能量/功率密度。
因此,需设计专门的预锂化添加剂作为高比容量的锂供体来消除最初的锂损失。在阳极和阴极上设计这种预锂化材料已经取得了一些进展。稳定的锂金属粉末和锂硅化物纳米粒子都被作为阳极预锂化添加剂。以减少阳极的不可逆容量损失。然而,负极预锂化材料具有低电位和高化学反应性,在锂离子电池中与应用环境、电解液溶剂、粘合剂和热处理工艺存在兼容性问题。阴极预锂化是补偿电池中锂损失的另一种途径。牺牲锂盐添加剂(例如,氮化物、碳氧化合物、二羧酸盐和酰肼)对第一次不可逆容量损失补锂。但是,这些添加剂的使用伴随着 N2、CO 或 CO2 的产生。类似地,Na3N 被用作钠离子电池中的添加剂,会释放N2。
此外,一些早期提出富锂化合物作为阴极添加剂(例如,Li2NiO2 和 Li6CoO4),其首次循环锂损失的有效补偿仍受到其低比容量(_300mAh/g)的影响。本文开发了一种化学反应路线,通过深度纳米级混合来合成氧化锂 (Li2O) 和金属 (M) 的纳米复合材料,以用于电池阴极预锂化。由于转化反应具有大电位滞后的独特特性,这种纳米复合材料中的锂在充电时很容易被脱出,而在放电时不会变回初始状态。因此,合成的 M/Li2O 纳米复合材料具有高“供体”锂离子容量。在全电池中,具有 Co/Li2O 添加剂的 LiFePO4 正极的整体容量得到显著提高。
Design for cathode prelithiation
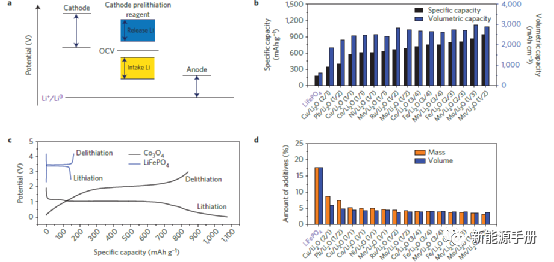
图1 | 用于锂离子电池的 M/Li2O 复合正极添加剂示意图。a,理想正极添加剂的潜在要求:在正极充电截止电位以下完全脱锂并在放电截止电位以下开始锂化。b,基于逆转化反应的各种M/Li2O复合材料的理论比容量和体积容量。c,MOs(例如 Co3O4)和现有商业正极(例如 LiFePO4)的典型电位曲线。M/Li2O 复合材料中的 Li 可以在低于阴极充电截止电位的情况下被脱出,但在高于截止放电电位的情况下不会被 MO 消耗。d,与使用额外数量的正极材料相比,实现完全补锂所需的 M/Li2O 正极预锂化材料的数量(在 LiFePO4/石墨全电池的情况下,初始不可逆锂损失为 30mAh g-1) .
以下几点是寻找有效的正极预锂化添加剂的指导方针。首先,良好的正极添加剂应具有比现有正极材料高得多的重量和体积的锂存储容量。例如,如果选择将现有正极材料加倍作为标准,则需要找到容量 >400mAh/g或 >1.2Ah/cm3 的预锂化添加剂。其次,添加剂应该能够在阴极充电期间在低于最大电位时脱出其储存的锂离子,但在阴极放电的最小电位下不能嵌入锂离子(图 1a)。也就是说,添加剂的脱锂电位低于最大阴极充电电位,而添加剂的锂化电位应低于最小阴极放电电位。这意味着添加剂的脱锂/锂化电位曲线应该有很大的滞后。第三,正极预锂化添加剂不应对电极材料、电解液和整个电池的稳定性产生负面影响。通常,这意味着需要相对较高的开路电压 (OCV)(图 1a)。第四,理想情况下,正极预锂化添加剂应在应用/生产条件下稳定,并与现有的工业电池制造工艺(如浆料混合、涂覆和烘烤)兼容。
考虑到上述标准,过渡金属氧化物 (MOs) 与锂的反应产物是正极预锂化添加剂的优秀候选者。在过去的十年中,MO(MxOy、M = Fe、Co、Ni、Mn 等)作为潜在的负极材料得到了深入研究。它们可以通过转化反应机制 (MxOy +2yLi+ + 2y+e-→ xM + yLi2O) 与锂反应,形成 M 和 Li2O 的纳米复合材料。M/Li2O 纳米复合材料存储的理论比容量是现有正极的理论比容量的四倍以上(例如,Co/Li2O(摩尔比,3/4)为 724mAh /g,Fe/Li2O(摩尔比,3/4)为 799mAh /g 2/3),以及 Mn/Li2O(摩尔比,1/2)的 935mAh /g。基于 M 和 Li2O 的密度,它们还可以提供高体积容量(例如,Co/Li2O(摩尔比,3/4)为 2,695mAh /cm3,Fe/Li2O 为 2,735mAh/cm3( Mn/Li2O(摩尔比,1/2)的摩尔比为 2/3)和 2,891mAh/cm3。
MOs 的转化反应通常表现出低于 1.2V 的锂化电位和在低于~3V 的电位下几乎完全脱锂,这表现出较大的充放电电压滞后。例如,图 1c 显示了 Co3O4 的实验第一次循环电化学锂化/脱锂电压曲线,其中锂化主要发生在 1.2 至 0.01V 之间,可以在 3V 以下提供 842mAh g-1 的非常高的锂离子容量。宽电压范围和大滞后使得单独的过渡氧化物作为良好的阳极或阴极材料并不理想。然而,过渡氧化物的这些特性使其成为优异的正极预锂化添加剂。现有正极材料的充电截止电位通常大于 4.0 V 与 Li/Li+(例如,LiFePO4 为 4.2V,LiCoO2 为 4.3V,图 1c),Li+可以轻松地从 M/ Li2O复合材料中脱出。同时,它们的放电截止电位高于 2.5V(例如,LiFePO4 为 2.5V,LiCoO2 为 3.0V,图 1c),仍远高于 MO 的锂化电位。
换句话说,作为正极添加剂的 M/Li2O 复合材料可以在正极的第一次充电过程中贡献大量的锂,而它们的锂化反应不会在正极放电过程中发生。使用 M/Li2O 复合材料作为预锂化添加剂的影响如图 1d 所示,该图显示了在 LiFePO4/石墨全电池中补偿首次循环 的Li 损失(例如,30mAh /g)必须额外加载 18% 的 LiFePO4 正极材料。相比之下,仅需要 3-5% 的 M/Li2O 正极添加剂来抵消这种初始锂损失(图 1d)。相应地,比能量密度和体积能量密度分别增加到 8-13% 和 11-14%。
Electrochemistry of the Co/Li2O nanocomposite
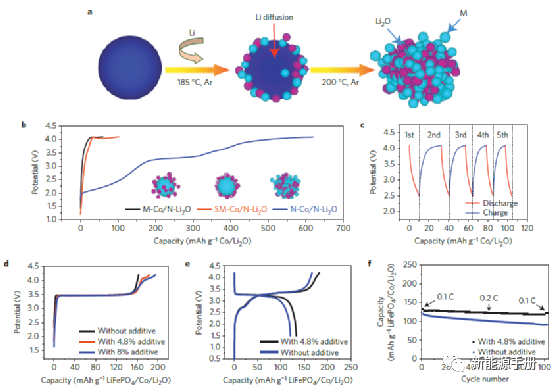
图2 | N-Co/N-Li2O 复合材料的制备和电化学特性。a,N-M/N-Li2O复合材料的制备过程示意图。MOs 被用作起始材料,并通过与熔融锂的化学反应原位转化为 N-M/N-Li2O 复合材料。b,由各种 Co/Li2O 纳米复合材料制成的电极的初始充电电位曲线:M-Co/N-Li2O 复合材料、SM-Co/N-Li2O 复合材料和 N-Co/N-Li2O 复合材料。c,第一次充电过程后 N-Co/N-Li2O 电极的充电/放电电位曲线。d,在半电池配置中具有不同量 N-Co/N-Li2O 添加剂的 LiFePO4 电极的初始充电电位曲线。e,f,含和不含 N-Co/N-Li2O 添加剂的 LiFePO4/石墨全电池的初始充电/放电电位曲线(e)和循环性能(f)。正极的比容量基于 LiFePO4 和 N-Co/N-Li2O 添加剂的重量进行评估。
本工作为 M/Li2O(M:Co、Fe、Ni 等)纳米复合材料开发了一种通用的一步合成方法(图 2a),并证明它们可成功作为正极添加剂,以达到有效补锂的目的。通过在 Ar 气氛下将 MxOy 与熔融锂混合,合成了纳米尺寸N-M/N-Li2O复合材料。根据转化反应方程式(MxOy + 2yLi→xM + yLi2O)设定起始 MxOy 和 Li 的摩尔比。锂金属箔在 185°C 下熔化,并在机械搅拌下与 MxOy 反应 20 分钟。然后,将温度进一步升至 200 ℃并保持 2 小时以使其完全反应。最后,获得了包含嵌入纳米级 Li2O 基质中的纳米级金属颗粒的均匀纳米复合材料(图 2a)。这些 M/Li2O 纳米复合材料通过常规浆料处理以形成电池电极(参见方法)。
纳米级 Co/纳米级 Li2O(N-Co/N-Li2O;摩尔比,3/4)复合材料的电化学性能(图 2b,c)正如预期的那样,在 4.1 和 2.5V 之间的电位范围内的第一个循环中提供了 619mAh/g 的高充电比容量和 10mAh/g 的低放电比容量,满足电压标准作为阴极预锂化添加剂。为了比较,还研究了另外两种 Co/Li2O 纳米复合材料的电化学性能,包括微米级 Co/纳米级 Li2O(M-Co/N-Li2O)和亚微米级 Co/纳米级 Li2O复合材料(图 2b)。由于 Co 的粒径较大以及 Li2O 和 Co 颗粒之间的松散接触(稍后讨论),它们表现出更高的充电电位 (_4.1V) 和更低的比充电容量 (<100mAh/g)。这些结果说明 Co 和 Li2O 需彻底纳米级混合的必要性。需要说明的是,M-Co/N-Li2O 复合材料的浆料涂覆和电极烘烤是在环境条件下进行的。暴露在大气中 8 小时后,比容量为 568mAh/g,仅比初始值低 51mAh/g。即使在两天后,比容量仍达到 418mAh/g,表明与传统锂离子电池制造环境兼容性好(补充图 3)。
通过一步化学反应制备的 N-Co/N-Li2O 复合材料的锂脱出电位(图 2b)略高于 Co3O4 的电化学锂化产物(图 1c)。这可能是由这两种方法生产的 Co/Li2O 纳米复合材料的不同晶粒尺寸造成的。与电化学锂化产生的对应物(图 1c)相比,化学合成的 N-Co/N-Li2O 复合材料表现出 1.8V 的高 OCV(图 2b),该值处于现有的正极材料稳定的电压范围内。因此,它可以很容易地与各种正极材料混合,且在电极加工过程中对其化学和结构稳定性的负面影响可以忽略不计。此外,N-Co/N-Li2O 电极在第一次循环后几乎失去了所有容量,这表明在第一次充电期间提供锂离子后,这些纳米复合材料对阴极中的活性电化学过程没有贡献(图 2c) .所有这些特性使 N-Co/N-Li2O 正极添加剂能够有效补偿现有锂离子电池的首次循环容量损失。
图 2d 显示了具有不同数量的 N-Co/N-Li2O 正极预锂化材料的 LiFePO4 正极和 Li 金属负极半电池的充电电位曲线。除非另有说明,比容量是基于 LiFePO4 和 N-Co/N-Li2O 复合物的总重量计算的。由原始商用 LiFePO4 粉末制成的电极可提供 164mAh/g的初始充电容量。使用 4.8% 的 N-Co/N-Li2O 添加剂(基于整个阴极),第一次循环比充电容量达到 183mAh/g(高出 12%)。当使用 8% N-Co/N-Li2O 添加剂时,初始比充电容量高达 195mAh/g(高出 19%)。可以清楚地观察到原始 LiFePO4 电荷平台上方的电位斜率,这与原始 N-Co/N-Li2O 复合材料的脱锂过程一致(图 2b、d)。含有大量 N-Co/N-Li2O 添加剂的 LiFePO4 电极清楚地显示了添加剂在不同电位范围内的响应(添加剂/LiFePO4 的重量比为 1/6,补充图 4)。
同时,在锂金属半电池中有和没有 N-Co/N-Li2O 添加剂的 LiFePO4 正极显示出高比放电容量和稳定的循环性能(补充图 5),表明 N-Co/N-Li2O 添加剂在循环过程中对正极稳定性的负面影响可以忽略不计。与原始阳极相比,具有预锂化材料的阳极可以在其表面形成更好的钝化表面膜,这可能有助于阳极实现稳定的电化学性能。最近的一篇论文报道,通过阴极预锂化活化也可以在 LiNi0.5Mn0.3Co0.2O2 阴极表面形成稳定的表面膜,从而提高了 LiNi0.5Mn0.3Co0.2O2 阴极的循环稳定性。为了展示使用 N-Co/N-Li2O 添加剂的普遍性,我们还尝试了使用这种添加剂的 LiCoO2 和 LiNi0.6Co0.2Mn0.2O2 正极,以证明其锂“供体”效应。补充图 6 显示了 LiCoO2 和 LiNi0.6Co0.2Mn0.2O2 的第一次充电电位曲线,有和没有 N-Co/N-Li2O 添加剂。添加剂的锂“供体”效应清楚地通过变化得到证实由添加剂引起的电位斜率和增加的总容量(基于正极材料和添加剂的质量)。
具有 4.8% N-Co/N-Li2O 添加剂的 LiCoO2 电极的初始充电容量为 190.8mAh/g(比原始 LiCoO2 电极的 170.2mAh/g 高 12%)。添加 4.8% N-Co/N-Li2O 添加剂后,LiNi0.6Co0.2Mn0.2O2 正极的第一次循环比充电容量达到 208.0mAh/g(比原始 LiNi0.6Co0.2Mn0 高 9% .2O2 电极)。含有和不含添加剂的电极表现出相似的循环稳定性,表明 N-Co/N-Li2O 添加剂对各种正极稳定性的负面影响可以忽略不计。
在一个全电池中,所有的锂都来自正极材料。由于第一次循环充电过程中的不可逆反应,在放电过程中部分锂不能回到正极,降低了电池的能量密度。理想情况下,当正极添加剂的用量得到优化时,全电池正极的放电容量可以达到与锂金属半电池相同的值。为了进一步评估 N-Co/N-Li2O 复合材料的锂补偿效果,进行了 LiFePO4/石墨全电池的电化学表征。如图 2e 所示,未添加 N-Co/N-Li2O 正极添加剂的原始 LiFePO4/石墨全电池的可逆放电容量仅为 120mAh/g。
相比之下,总阴极中含有 4.8 wt% N-Co/N-Li2O 阴极添加剂的 LiFePO4/石墨全电池可提供 133mAh/g(高 11%)的可逆放电容量,基于LiFePO4 和 N-Co/N-Li2O 复合材料,这与 LiFePO4/Li 金属半电池中获得的值相同(补充图 5)。当根据 LiFePO4 的重量计算时,可逆放电容量高达 141mAh g-1(补充图 7)。含和不含 N-Co/N-Li2O 添加剂的 LiFePO4/石墨全电池的第一次循环充电电势曲线在低充电电势 (~3.3V) 下非常吻合,并且观察到延长的充电平台和斜率具有高充电电位 (~3.3V) 的 Co/Li2O 阴极添加剂的电池。
相应地,具有阴极添加剂的电池在其放电过程中显示出延长的平台。这些结果证实,N-Co/N-Li2O 添加剂释放的容量有效地补偿了全电池的第一次循环容量损失。整个锂离子电池的整体容量和能量密度都有了明显的提高。此外,具有 4.8% 阴极添加剂的全电池在循环时表现出稳定的电位曲线和显着提高的容量保持率,100 次循环中每个循环的平均容量衰减为 0.07%(图 2f 和补充图 8),具有可比性或比不含 N-Co/N-Li2O 添加剂的参考原始 LiFePO4/石墨全电池更好的稳定性。
Structure characterizations and in situ TEM measurement

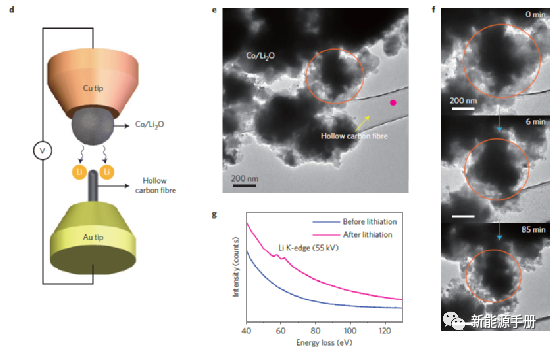
图 3 | N-Co/N-Li2O 复合材料在锂脱出过程中的结构和演变。a,N-Co/N-Li2O 复合材料的 STEM 图像,显示 Co 纳米颗粒均匀嵌入 Li2O 基质中。b,c, HRTEM 图像 (b) 和 Co 颗粒的相应条纹 (c),显示其结晶度和小粒径。d,e,原位 TEM 设备的示意图(d)和配置(e)。Cu 尖端上的 N-Co/N-Li2O 复合材料用作工作电极,模板制造的中空碳纤维用作对电极。f,g,延时 TEM 图像 (f) 和 EELS 光谱 (g)。施加偏压后,锂从 N-Co/N-Li2O 工作电极中脱出并转移到碳对电极,导致体积收缩。N-Co/N-Li2O 颗粒聚集体用红色圆圈标记,并观察到其体积收缩。EELS 光谱是在 N-Co/N-Li2O 复合材料脱锂前后,在中空碳纤维处拍摄的,用 e 中的粉红色点标记。结果表明锂从工作电极转移到对电极。
接下来,我们试图研究 N-Co/N-Li2O 复合材料的结构及其在电化学锂脱出过程中的演变。X 射线光电子能谱(XPS)、电子能量损失谱(EELS)和 X 射线衍射(XRD)的结果表明产物中 Co 纳米颗粒的结晶性质和 Li2O 的无定形结构(补充图 9_11)。起始 Co3O4 包含微米级二次粒子聚集体,初始粒径为 50_100nm(补充图 12)。与锂发生化学反应后,微观结构发生显着变化,但其整体形状得以保留(补充图 13)。透射电子显微镜(TEM)结果显示,起始颗粒在反应后完全转化为嵌入 Li2O 基质中的 5nm Co 纳米颗粒(补充图 14)。为了深入了解复合材料中金属 Co 颗粒和 Li2O 的分布,进行了扫描 TEM (STEM)。如图 3a 所示,可以清楚地观察到 STEM 图像中的明暗对比。灰色区域可以分配给 Li2O。光斑表明存在大量 Co 纳米颗粒。值得注意的是,金属 Co 纳米晶体均匀地嵌入 Li2O 基质中。金属 Co 的结晶度由高分辨率 TEM(HRTEM)证实(图 3b,c)。
同时,通过 STEM/能量色散 X 射线光谱(EDX)和 STEM/EELS 元素映射分析(补充图 15)验证了复合材料中 Li2O 和 Co 的均匀分布。我们认为,Co 颗粒的小尺寸及其在 Li2O 中的均匀分布,以及 Co 和 Li2O 之间的密切接触,对于从 N-Co/N-Li2O 复合材料中完全电化学脱出 Li 至关重要。转化反应复合材料的电化学活性受微观结构和粒径的强烈影响。与小粒度的复合材料相比,大粒度的复合材料显示出更高的锂脱出电位和更低的锂离子容量。与由电化学驱动的转化反应产生的金属纳米颗粒相比,这些 Co 颗粒具有稍大的粒径和更高的结晶度 (-2 nm),这解释了为什么N-Co/N-Li2O 复合材料具有更高的 OCV和电荷电位高于从电化学驱动的转化反应中获得的电位。
相比之下,由于 Co 颗粒大得多,Co 和 Li2O 之间的接触更松散,M-Co/N-Li2O 复合材料和 SM-Co/N-Li2O 复合材料表现出更高的电荷电位,并提供非常低的比电荷容量。施加的电位范围(图 2b 和补充图 16)。为了了解从 N-Co/N-Li2O 复合材料中脱出锂的过程,我们进行了原位 TEM 电化学测量。原位 TEM 电化学装置的设置基于先前的研究。如图 3d、e 所示,我们的电化学微电池由 N-Co/N-Li2O 复合材料作为工作电极和模板制造的中空碳纤维作为对电极组成。工作电极表面的 Li2O 层也充当固体电解质。施加偏压以驱动逆向转化反应并将锂从工作电极脱出到碳对电极。在脱锂过程中记录了 N-Co/N-Li2O 颗粒聚集体的一系列 TEM 图像(图 3f 和补充视频 1)。
结果表明,在施加偏压后,初始粒子立即开始收缩,表明锂正在被脱出。考虑到 N-Co/N-Li2O 颗粒聚集体的初始尺寸,脱锂后保留不到其初始体积的一半。此外,在脱锂过程之前和之后,在碳对电极上拍摄的 EELS 光谱有效地证实了锂从 N-Co/N-Li2O 工作电极转移到碳对电极的事实(图 3g)。在锂脱出过程中,Co 可能会经历多种氧化态,例如 CoO、Co3O4 和其他一些可能的过渡态。XPS 研究证实了半电荷状态下的中间 CoO(补充图 17)。Co 的多个中间相和氧化态可能导致从 Co/Li2O 纳米复合材料中脱出锂过程中的多步电压趋势(图 2b)。脱锂后得到的产物经XPS证实为Co3O4,表明其逆向转化反应机理:3Co+4Li2O→Co3O4 + 8Li(补充图 17)。
Generalization to other metal/Li2O nanocomposites
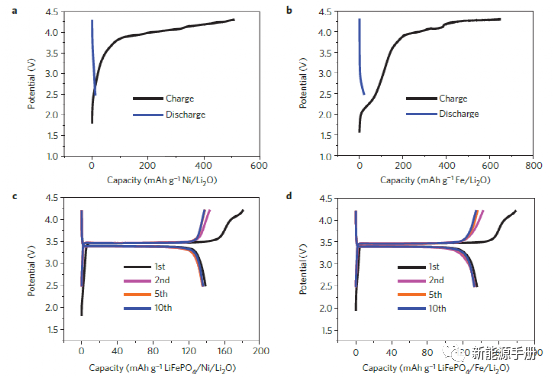
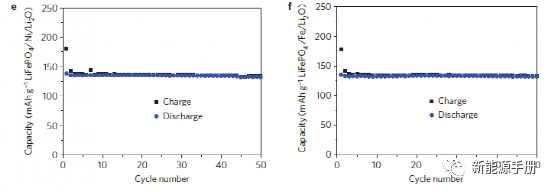
图 4 | 推广到其他 N-M/N-Li2O 复合材料。a,b,原始 N-Ni/N-Li2O(a)和 N-Fe/N-Li2O 电极(b)的初始充电/放电电位曲线。c,d,半电池配置中含有 4.8% N-Ni/N-Li2O (c) 和 N-Fe/N-Li2O (d) 添加剂的 LiFePO4 电极的放电/充电电位曲线。e,f,含 4.8% N-Ni 的 LiFePO4 电极的循环性能
为了展示使用 N-M/N-Li2O 复合材料作为高容量正极添加剂的通用性,还使用相同的合成程序制备了 N-Ni/N-Li2O 和 N-Fe/N-Li2O 复合材料。XRD证实它们由M 和 Li2O组成(补充图 18)。分别为 N-Ni/N-Li2O 和 N-Fe/N-Li2O 复合材料制备工作电极。如图 4a、b 所示,N-Ni/N-Li2O 和 N-Fe/N-Li2O 电极在第一次循环充电过程中表现出不同的电位分布,这可能是由于 M 原子和粒径之间的差异.与 N-Co/N-Li2O 复合材料类似,它们具有高初始 OCV(高于 1.5V)并提供分别为 506 和 631mAh/g 的高充电容量,以及 11 和 19mAh /g的极低放电容量1,分别(图4a,b)。具有两种添加剂的 LiFePO4 电极都经历了循环(图 4c、d)。正如预期的那样,它们的第一次循环充电容量显着提高。含 4.8% N-Ni/N-Li2O 添加剂的电极的初始充电容量为 180mAh/g,含 4.8% N-Fe/N-Li2O 复合材料的电极的初始充电容量为 178mAh/g。这些容量比没有任何预锂化添加剂的 LiFePO4 电极高 10%。此外,这些电极还显示出非常好的循环稳定性(图 4e、f)。
Conclusions
提出了一种阴极预锂化的设计原则,以补偿锂离子电池中首效锂损失。通过利用转化反应的高比容量和大电位滞后的独特特性,展示了一类表现出高预锂化效率M 和 Li2O 的纳米级混合物。使用这种阴极预锂化添加剂,LiFePO4/石墨全电池的比容量和能量密度得到显着提高。制成的高容量预锂化材料纳米复合材料,可兼容于现有的工业电池制造工艺。
Methods
材料合成。将 Co3O4 纳米颗粒(2mmol,99.5%,Sigma-Aldrich)与熔融锂金属(16mmol,99.9%,Alfa Aesar)在 185 ℃下反应 20 分钟,在 200 ℃下反应 2 h 在充满氩气的手套箱中连续机械搅拌(水分含量低于 0.1 ppm,氧气含量低于 3.0 ppm)。为了消除残留的锂金属,合成的复合材料在使用前储存在干燥的空气中。使用相同的程序制备 N-Ni/N-Li2O 和 N-Fe/N-Li2O 复合材料,以 NiO(8mmol,99.8%,Sigma-Aldrich)和 Fe3O4(2mmol,97%,Sigma-Aldrich)纳米粒子作为起始材料。MOs和Li的摩尔比是根据它们的反应设计的(MxOy + 2yLi !xM + yLi2O)。通过将商业 Li2O 颗粒(97%,Sigma-Aldrich)和 Co 颗粒(99.8%,Sigma-Aldrich)分别进行机械研磨技术,获得 Li2O 纳米颗粒和微米级钴颗粒。将得到的 Li2O 纳米粒子和微米级 Co 粒子按照 4:3 的摩尔比均匀混合,得到 M-Co/N-Li2O 复合材料。在对 M-Co/N-Li2O 复合材料进行进一步机械研磨后,制备出 SM-Co/N-Li2O 复合材料。
表征。 XRD是使用 Panalytical X'pert 衍射仪和 Ni 过滤的 Cu K_ 辐射 (_ = 1.5406 Å) 进行的。XPS 分析是用 PHI Versa Probe 5000 系统(物理电子)进行的。FEI Titan 80_300 环境 TEM 用于 HRTEM 和 STEM 图像、EDS 和 EELS 映射收集以及原位 TEM 测量。Nano factory Instruments Dual-Probe STM-TEM 原位样品架用于演示 N-Co/N-Li2O 复合材料的脱锂过程。测量过程中,在 N-Co/N-Li2O 工作电极和中空碳纤维对电极之间施加 6V 的相对偏压,引起逆转换反应,从工作电极中脱出锂并将其转移到对电极。在碳电极上拍摄N-Co/N-Li2O 复合材料脱锂前后的EELS 光谱。
电化学测量。在 Arbin Battery Cycler 仪器上使用 2032 型纽扣电池(MTI Corporation)评估电池性能。电池在充满氩气的手套箱中组装,使用 1M LiPF6 在碳酸亚乙酯 (EC) 和碳酸二乙酯 (DEC) (1:1 v/v) 的混合物中作为电解质,使用 Celgard 2300 膜作为隔膜。通过在 N-甲基-2-吡咯烷酮 (NMP) 溶剂中混合活性材料、炭黑和聚偏二氟乙烯 (PVDF) 粘合剂,在环境条件下进行用于电极制造的浆料涂层。然后将电极在 60°C 下真空干燥。M/Li2O 电极由重量为 60% 的 M/Li2O 复合材料、30% 的炭黑和 10% 的 PVDF 粘合剂组成,典型负载量为 _1mg cm{2。商业 LiFePO4 粉末(MTI Corporation)和合成的正极添加剂以不同的重量比混合作为活性混合正极材料。LiFePO4 电极由 80% 的这些混合阴极材料、10% 的炭黑和 10% 的 PVDF 制备。它们的典型质量负载为 ~5mg/cm2。通过将石墨粉(MTI Corporation)、炭黑和 PVDF 以 8:1:1 的质量比混合制成石墨电极。阳极的活性负载为 2.3mg/cm2。用于全电池测试的负极与正极的容量比(N/P比)为1.02。M/Li2O/Li 金属半电池充电至 4.1/4.3V,放电至 2.5V,电流密度为 50mAgƀ1。LiFePO4/Li 金属半电池的恒电流充放电测量在截止电位范围 2.5-4.2V下进行。LiFePO4/石墨全电池的截止电位范围为 1.5-4.2V。LiFePO4 电极的电流密度第一次循环为 0.1 C,随后循环为 0.2 C。
参考资料:https://www.nature.com/articles/nenergy20158
新能源汽车的快速发展带动了动力电池的高速增长。动力电池生产流程一般可以分为前段、中段和后段三个部分。其中,前段工序包括配料、搅拌、涂布、辊压、分切等,中段工序包括卷绕/叠片、封装、烘干、注液、封口、清洗等,后段主要为化成、分容、PACK等。材料方面主要有正负极材料,隔膜,电解液,集流体,电池包相关的结构胶,缓存,阻燃,隔热,外壳结构材料等材料。 为了更好促进行业人士交流,艾邦搭建有锂电池产业链上下游交流平台,覆盖全产业链,从主机厂,到电池包厂商,正负极材料,隔膜,铝塑膜等企业以及各个工艺过程中的设备厂商,欢迎申请加入。

长按识别二维码关注公众号,点击下方菜单栏左侧“微信群”,申请加入群聊
